利用細胞表面特異性受體及蛋白標志物,識別并捕捉特定組織及特定生理病理狀態下的細胞,對于疾病診斷、靶向治療都有非常重要的意義。糖蛋白及糖結合蛋白作為細胞-細胞、細胞-微環境相互作用的重要媒介,隨著糖組學的發展,其重要性也日益受到重視。
針對現有化學糖生物學檢測手段技術繁復、耗時長、成本高的技術缺陷,中國科學院上海藥物研究所的研究人員創新發展了“帶電的糖”系列分子探針,將具備高電化學活性的醌類基團與糖類偶聯,并應用有序分子自組裝手段構建了可在分子水平選擇性識別凝集素的糖醌金電極單分子層(J. Am. Chem. Soc. 2011, 133:3649);進一步應用高效的點擊化學手段將半乳糖與蒽醌基團偶聯,并使用更為經濟、制備簡易,且具備優異電學性能的石墨烯材料組成可攜式工作電極,通過蒽醌與石墨烯的π-堆疊有序自組裝構建了含有蒽醌電化學信號的探針體系,實現了對表達ASGPr(脫唾液酸糖蛋白受體)的肝癌活細胞的靈敏捕捉,并驗證了當ASGPr被基因敲除后,相應電化學感應信號明顯削弱(Sci. Rep. 2013, 3: 2293)。
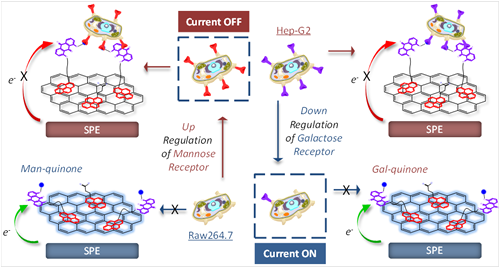
在此基礎上,研究人員在糖蒽醌骨架上通過點擊化學引入了芘作為更為牢固的石墨烯結合基團,使糖基蒽醌可更為靈活地排布于電極表面,優化與細胞表面受體的識別能力。通過這一體系,優化和拓展了對于不同細胞受體表達量的實時探測。引入芘的半乳糖-石墨烯電極可高效、特異地捕捉特異性表達ASGPr的肝癌hepG2活細胞。此外甘露糖覆蓋的電極可對經IL-4刺激單核細胞RAW264.7誘導分化的M2型巨噬細胞(高表達特異性表面凝集素標志物甘露糖受體MR)產生顯著電化學信號變化,而對不表達甘露糖受體的M1型巨噬細胞、單核細胞及肝、子宮頸及結腸等組織來源對照細胞(HepG2, Hela, HCT116)不產生響應信號。此項研究成果發表于英國皇家化學會最新一期的Chemical Science(2015, 6:1996)。
上述系統工作為糖與受體蛋白的細胞水平探測提供了高效電化學工具。
研究工作由上海藥物所研究員李佳、臧奕與華東理工大學長江學者龍億濤及副研究員賀曉鵬合作完成。項目獲得了“973”計劃、國家基金委創新群體、國家自然科學杰出青年基金及上海市科委等資助。
轉自石墨烯網論壇www.graphenes.net
南京吉倉納米科技有限公司網絡中心




